Sönmüş ve sönmemiş kireç arasındaki formüller nelerdir?
Sönmüş ve sönmemiş kireç, inşaat sektöründe temel bileşenlerdir. Kalsiyum oksit ve kalsiyum hidroksit olarak iki formda bulunan bu maddeler, çeşitli kimyasal süreçler ve endüstriyel uygulamalar için kritik öneme sahiptir. Çalışmada, her iki bileşiğin formülleri, özellikleri ve kullanım alanları detaylı bir şekilde ele alınmaktadır.
Sönmüş ve Sönmemiş Kireç Arasındaki Formüller Nelerdir?Sönmüş ve sönmemiş kireç, inşaat ve yapı sektörlerinde yaygın olarak kullanılan iki temel bileşiktir. Bu iki madde, kalsiyum oksit (CaO) ve kalsiyum hidroksit (Ca(OH)₂) arasında bir geçişi temsil eder. Bu makalede, sönmüş ve sönmemiş kireç arasındaki kimyasal formülleri, üretim süreçlerini, özelliklerini ve kullanım alanlarını detaylı bir şekilde inceleyeceğiz. 1. Sönmemiş Kireç (Kalsiyum Oksit) Nedir?Sönmemiş kireç, kalsiyum karbonatın (CaCO₃) ısıtılması ile elde edilen bir bileşiktir. Bu işlem, kalsiyum karbonatın termal ayrışması ile gerçekleşir.
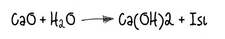
Bu işlemde, kalsiyum karbonat 900-1000 °C arasında ısıtıldığında kalsiyum oksit ve karbondioksit gazı açığa çıkar. Elde edilen sönmemiş kireç, yüksek sıcaklıklara dayanıklı ve alkalin bir bileşiktir. 2. Sönmüş Kireç (Kalsiyum Hidroksit) Nedir?Sönmüş kireç, sönmemiş kireç ile suyun tepkimeye girmesi sonucu oluşan bir bileşiktir. Bu işlem, hidratasyon olarak adlandırılır ve aşağıdaki şekilde ifade edilir:
Sönmüş kireç, kalsiyum hidroksit olarak da bilinir ve genellikle beyaz toz halinde bulunur. Su ile karıştırıldığında, süspansiyon oluşturur ve bu ortamda bazik özellikler gösterir. 3. Sönmüş ve Sönmemiş Kireç Arasındaki Farklar Sönmüş ve sönmemiş kireç arasındaki temel farklar şunlardır:
4. Kullanım Alanları Sönmemiş ve sönmüş kireç, çeşitli endüstriyel uygulamalarda geniş bir yelpazeye sahiptir. Bunlardan bazıları şunlardır:
5. Sonuç Sönmüş ve sönmemiş kireç, yapı ve inşaat sektöründe kritik öneme sahip iki bileşiktir. Kimyasal formülleri, üretim süreçleri ve kullanım alanları bakımından önemli farklılıklar taşırlar. Sönmemiş kireç, daha reaktif bir bileşen olarak, inşaat ve üretim süreçlerinde geniş bir kullanım alanı bulurken; sönmüş kireç, su arıtma ve tarım gibi alanlarda önemli bir rol oynamaktadır. Bu iki bileşiğin doğru bir şekilde kullanılması, hem ekonomik hem de çevresel sürdürülebilirlik açısından büyük önem taşır. |